
L'ACTUALITÉ EN CANCÉROLOGIE VUE PAR GUSTAVE ROUSSY
Newsletter #2 - novembre 2020
ORL
Le Debio 1143, un nouveau traitement prometteur, en association avec la radio-chimiothérapie, dans un essai de phase II
Yungan Tao, Marion Classe.
Progression de la maladie ralentie, survie sans progression améliorée : un inhibiteur des protéines inhibitrices de l’apoptose confirme son intérêt contre des cancers ORL de mauvais pronostic.
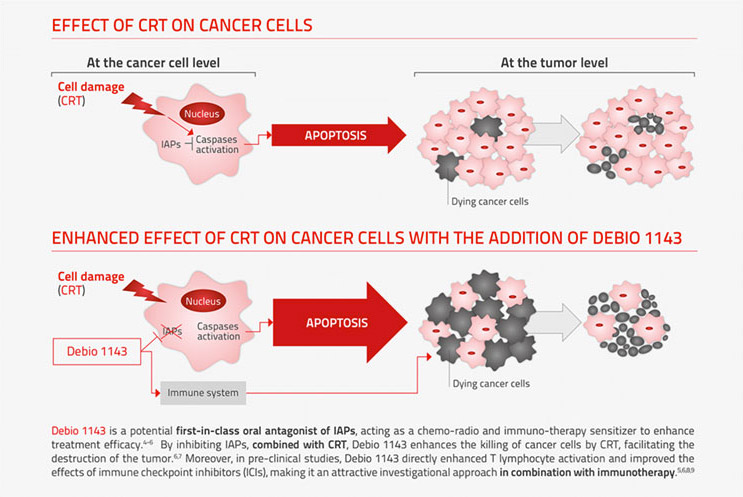
Après une étude de phase I prometteuse1, l’étude de phase II comparant l’efficacité et la tolérance du Debio 1143 contre placebo s’est révélée positive chez des patients atteints d'un carcinome épidermoïde ORL de stade locorégional avancé et ayant des antécédents de tabagisme important2. Le Debio 1143 (xevinapant) est un inhibiteur des IAP, inhibiteurs des protéines de l’apoptose. Il renforce l’efficacité des chimios et radiothérapies en favorisant la mort programmée des cellules et en renforçant l’immunité antitumorale. Ce candidat-médicament ou un placebo ont été ajoutés à la radio-chimiothérapie standard à haute dose de cisplatine chez 96 patients randomisés (48 dans chaque groupe). La majorité de ces patients étaient de gros fumeurs présentant un cancer de l’oropharynx non lié au virus HPV.
Le Dr Yungan Tao, oncologue-radiothérapeute à Gustave Roussy, a activement participé à cette étude multicentrique menée par le GORTEC (Groupe Oncologie Radiothérapie Tête et Cou) et Debiopharm. Les résultats sont publiés dans le Lancet Oncology de septembre 2020. Ils montrent que le taux de contrôle locorégional à 18 mois après radiothérapie s'est amélioré de 21% (OR = 2,69 ; 95 % CI [1,13–6,42], p = 0,026) dans le groupe traité avec le Debio1143.
Après presque deux ans de suivi, la survie médiane sans progression était de 16,9 mois pour le groupe placebo et n’était pas encore atteinte dans le groupe Debio1143 (HR = 0,37 ; p = 0,007). La survie globale médiane n'était pas encore atteinte dans aucun des deux groupes (HR = 0,65 ; p = 0,243). Des événements indésirables (EI) de grade ≥3 ont été signalés chez 85 % des patients du groupe Debio 1143 et 87 % patients du groupe placebo. La dysphagie, la mucite et l’anémie de grade ≥3 étaient plus fréquentes avec Debio 1143. Deux patients (4 %) ont présenté des EI de grade 5 dans le groupe placebo.
Il s'agit du premier schéma thérapeutique avec une efficacité supérieure à la radio-chimiothérapie cisplatine à haute dose dans un essai randomisé. Ces résultats suggèrent que l'inhibition des protéines inhibitrices de l’apoptose est une approche nouvelle prometteuse dans cette population de mauvais pronostic et justifie une confirmation dans une étude de phase III.
Références :
- Le Tourneau C, Tao Y, Gomez-Roca C, Cristina V, Borcoman E, Deutsch E, Bahleda R, Calugaru V, Modesto A, Rouits E, Gollmer K, Vuagniaux G, Crompton P, Zanna C, Szyldergemajn S, Delord JP, Bourhis J. Phase I trial of Debio 1143, an antagonist of inhibitor of apoptosis proteins, combined with cisplatin-chemoradiotherapy in patients with locally advanced squamous cell carcinoma of the head & neck. Clin Cancer Res. 2020 Sep 29:clincanres.0425.2020. doi: 10.1158/1078-0432.CCR-20-0425. Epub ahead of print. PMID: 32994295.
- Sun XS, Tao Y, Le Tourneau C Pointreau Y, Sire C, Kaminsky MC, Coutte A, Alfonsi M, Boisselier P, Martin L, Miroir J, Ramee JF, Delord JP, Clatot F, Rolland F, Villa J, Magne N, Elicin O, Gherga E, Nguyen F, Lafond C, Bera G, Calugaru V, Geoffrois L, Chauffert B, Zubel A, Zanna C, Brienza S, Crompton P, Rouits E, Gollmer K, Szyldergemajn S, Bourhis J. Debio 1143 and high-dose cisplatin chemoradiotherapy in high-risk locoregionally advanced squamous cell carcinoma of the head and neck: a double-blind, multicentre, randomised, phase 2 study. Lancet Oncol. 2020 Sep;21(9):1173-1187. doi: 10.1016/S1470-2045(20)30327-2. Epub 2020 Aug 3. PMID: 32758455.
Oncologie thoracique
Cibler la mutation KRASG12C : premiers résultats positifs
Antonin Levy.
Deux essais cliniques de phase 1 et 1/2 témoignent des bénéfices de différents inhibiteurs de KRAS dans le cancer bronchique non à petites cellules et le cancer colorectal. Cibler ces inhibiteurs jusqu’alors jamais ciblés quelque soit le type de cancer est de bon augure pour d’autres molécules de cette famille déjà à l’étude à Gustave Roussy.
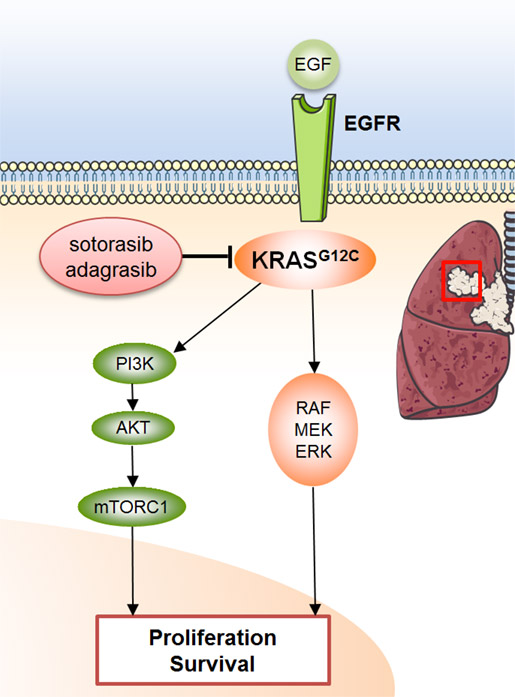
La voie de signalisation intracellulaire RAS/MAPK intervient dans la régulation de la prolifération, de la survie, de la différenciation et de la migration cellulaire. Elle est anormalement activée dans de nombreux cancers via l’activation de récepteurs membranaires tels que l’EGFR, mais aussi en cas de mutations somatiques au niveau de gènes codant pour la protéine RAS.
La mutation activatrice KRAS p.G12C est une des plus fréquentes dans les cancers bronchiques non à petites cellules (CBNPC), survenant dans 13-14 % des cas (pour seulement 1 à 4 % dans le cancer colorectal). La mutation glycine-cystéine en position 12 (G12C) favorise la forme active de la protéine KRAS, résultant en une oncoprotéine KRAS liée au GTP et à la prolifération / survie des cellules tumorales. La cystéine mutée réside à côté d'une poche (P2) de la région switch II. La poche P2 est présente uniquement dans la conformation inactive liée au GDP de KRAS et a été exploitée pour établir des inhibiteurs covalents irréversibles de KRAS G12C. Le développement thérapeutique pourrait être dans un premier temps limité au mutant G12C car la réaction covalente se produit spécifiquement avec le groupe thiol du résidu cystéine.
Les premiers résultats attendus de deux inhibiteurs oraux spécifiques irréversibles de KRASG12C viennent d’être communiqués.
L’étude de phase 1 CodeBreaK100, publiée dans le New England Journal of Medicine1, a évalué le sotorasib (Amgen) chez 129 patients lourdement prétraités (médiane de trois lignes de traitements antérieurs) atteints de différents cancers, principalement CBNPC (46 %) et cancer colorectal (33 %). Aucune toxicité dose-limitante n’a été observée. Des effets secondaires ont été signalés chez 73 patients (56,6 %) et 15 (11,6 %) ont présenté une toxicité de grade 3 ou 4 (cytolyse hépatique, diarrhées, anémie). Le taux de réponse objective était de 32,2 % pour les patients atteints de CBNPC contre 7,1 % pour ceux atteints de cancer colorectal et la durée médiane de survie sans progression de 6,3 mois pour les premiers et de 4 mois pour les seconds.
Les résultats concernant les patients atteints de CBNPC mutés KRAS p.G12C inclus dans l’essai de phase 1/2 KRYSTAL-1 évaluant l’adagrasib (Mirati Therapeutics) ont été présentés au congrès ENA (EORTC-NCI-AACR) le mois dernier2. Parmi 79 patients, les effets secondaires de tout grade les plus fréquents étaient digestifs (nausées 54 %, diarrhées 48 %) et une hyponatrémie G3-4 a été observée chez deux patients. Le taux de réponse objective était de 45 % et le temps médian de traitement de 8,2 mois.
Plusieurs inhibiteurs de KRAS sont également à l’essai à Gustave Roussy et de nouvelles combinaisons de traitements seront étudiées.
Références :
- Hong DS, et al. KRASG12C Inhibition with Sotorasib in Advanced Solid Tumors. N Engl J Med. 2020;383:1207-1217.
- Janne PA, et al. KRYSTAL-1: Activity and Safety of Adagrasib (MRTX849) in Advanced/Metastatic Non–Small-Cell Lung Cancer (NSCLC) Harboring KRAS G12C Mutation. Eur J Cancer 2020; 138S2 : S1 (ENA 32th Symposium: Abstr #3LBA).
Cancers masculins
Le darolutamide augmente la survie des patients atteints d’un cancer de la prostate
Yohann Loriot.
Le cancer de la prostate résistant à la castration mais sans métastases constitue une situation atypique de la prise en charge des patients atteints de ce cancer. Il progresse tôt ou tard vers une forme métastatique incurable. De nouvelles stratégies sont imaginées pour lutter contre cette évolution défavorable.
Lors de ce scénario, la maladie évolue dans la mauvaise direction sans possibilité d’identifier clairement les zones tumorales actives avec les techniques d’imagerie habituelle. L’élévation sanguine du PSA conjuguée à l’absence de lésions à traiter rend la prise en charge des patients bien souvent asymptomatiques sujette à débat. L’attitude la plus fréquente privilégie une surveillance rigoureuse suivie d’une chimiothérapie lors de l’apparition quasi-inévitable des métastases.
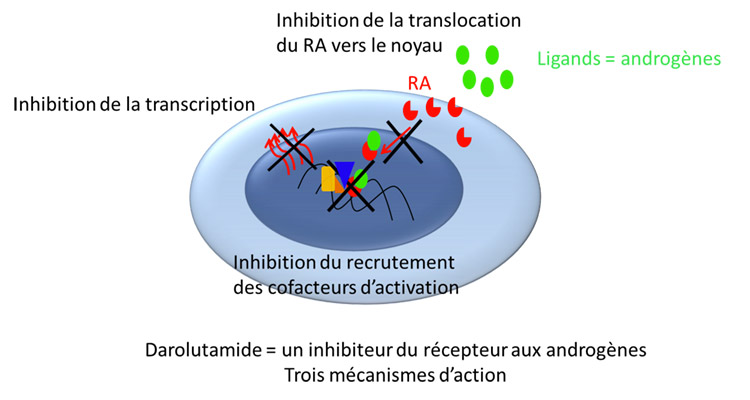
Dans un article paru dans le New England Journal of Medicine de Septembre 20201, le Pr Karim Fizazi, au nom d’une centaine d’investigateurs internationaux rapporte les résultats finaux de l’étude ARAMIS dont l’objectif était d’étudier l’intérêt du darolutamide dans cette situation clinique. Le darolutamide est un inhibiteur oral du récepteur aux androgènes de nouvelle génération développé en grande partie à Gustave Roussy, notamment au sein du Département des innovations et des essais précoces (Ditep)2. Cette étude montre que le traitement par le darolutamide de patients atteints de cancer de la prostate résistant à la castration mais sans métastase améliore leur survie par rapport à ceux traités par un placebo (HR = 0,69; 95 % CI [0,53 – 0,88]; P = 0,003). Le critère principal de l’étude ARAMIS, la survie sans métastase, avait déjà été analysé en 20193. Celle-ci était significativement prolongée chez les patients traités par darolutamide (40 mois contre 18 mois), ce qui avait conduit à une autorisation de mise sur le marché en Europe. Bien entendu, une amélioration de la survie globale était espérée afin de consolider l’intérêt de cette nouvelle molécule dans cette situation. Objectif atteint, donc, à l’issue de l’analyse finale de la survie globale, et ceci malgré la levée d’aveugle qui a permis à des patients inclus dans la bras placebo de recevoir à leur tour le darolutamide lors de la progression de la maladie. Le taux de survie à trois ans est de 83 % pour le groupe de patients traités dès le départ par le darolutamide alors qu’il n’est que de 77 % pour le groupe de patients ayant reçu le placebo. La diminution du risque de décès est de 31 %. En outre, la prescription de darolutamide permet de surseoir plus efficacement la survenue d’évènements osseux graves tels qu’une fracture et le recours à une chimiothérapie dont les contraintes sont plus importantes que celles induites par les hormonothérapies orales. Enfin, la tolérance des patients à ce médicament est correcte lorsque sont évalués les toxicités graves et les paramètres de qualité de vie.
ARAMIS confirme les résultats des autres essais qui posaient la même question avec des inhibiteurs de la même classe : l’enzalutamide (essai PROSPER)4 et l’apalutamide (essai SPARTAN)5. Les résultats paraissent donc crédibles et assoient le changement de prise en charge auxquels ils conduisent sur une base médicale solide. Toutefois, quand bien même ces traitements sont prescrits à un stade précoce de la maladie métastatique, ils ne guérissent pas les patients en raison de la survenue tôt ou tard de résistance secondaire qu’il faut appréhender. Enfin, les progrès de l’imagerie moléculaire, notamment avec les traceurs TEP-PSMA, conduisent inévitablement à une plus grande rareté de cette situation. D’autres études sont d’ores et déjà en cours en intégrant les stratégies de traitement des « niches », qui sont des sanctuaires tumoraux identifiés par ces imageries très sensibles, à l’aide de radiothéra-pies par exemple.
Références :
- Fizazi K, Shore N, Tammela TL, Ulys A, Vjaters E, Polyakov S, Jievaltas M, Luz M, Alekseev B, Kuss I, Le Berre MA, Petrenciuc O, Snapir A, Sarapohja T, Smith MR; ARAMIS Investigators. Nonmetastatic, Castration-Resistant Prostate Cancer and Survival with Darolutamide. N Engl J Med. 2020 Sep 10;383(11):1040-1049. doi: 10.1056/NEJMoa2001342. PMID: 32905676.
- Fizazi K, Massard C, Bono P, Jones R, Kataja V, James N, Garcia JA, Protheroe A, Tammela TL, Elliott T, Mattila L, Aspegren J, Vuorela A, Langmuir P, Mustonen M; ARADES study group. Activity and safety of ODM-201 in patients with progressive metastatic castration-resistant prostate cancer (ARADES): an open-label phase 1 dose-escalation and randomised phase 2 dose expansion trial. Lancet Oncol. 2014 Aug;15(9):975-85. doi: 10.1016/S1470-2045(14)70240-2. Epub 2014 Jun 25. PMID: 24974051.
- Fizazi K, Shore N, Tammela TL, Ulys A, Vjaters E, Polyakov S, Jievaltas M, Luz M, Alekseev B, Kuss I, Kappeler C, Snapir A, Sarapohja T, Smith MR; ARAMIS Investigators. Darolutamide in Nonmetastatic, Castration-Resistant Prostate Cancer. N Engl J Med. 2019 Mar 28;380(13):1235-1246. doi: 10.1056/NEJMoa1815671. Epub 2019 Feb 14. PMID: 30763142.
- Sternberg CN, Fizazi K, Saad F, Shore ND, De Giorgi U, Penson DF, Ferreira U, Efstathiou E, Madziarska K, Kolinsky MP, Cubero DIG, Noerby B, Zohren F, Lin X, Modelska K, Sugg J, Steinberg J, Hussain M; PROSPER Investigators. Enzalutamide and Survival in Nonmetastatic, Castration-Resistant Prostate Cancer. N Engl J Med. 2020 Jun 4;382(23):2197-2206. doi: 10.1056/NEJMoa2003892. Epub 2020 May 29. PMID: 32469184.
- Smith MR, Saad F, Chowdhury S, Oudard S, Hadaschik BA, Graff JN, Olmos D, Mainwaring PN, Lee JY, Uemura H, Lopez-Gitlitz A, Trudel GC, Espina BM, Shu Y, Park YC, Rackoff WR, Yu MK, Small EJ; SPARTAN Investigators. Apalutamide Treatment and Metastasis-free Survival in Prostate Cancer. N Engl J Med. 2018 Apr 12;378(15):1408-1418. doi: 10.1056/NEJMoa1715546. Epub 2018 Feb 8. PMID: 29420164.
Sénologie
Effet du dépistage mammographique à partir de 40 ans sur la mortalité due au cancer du sein
Anna Ilenko, Benjamin Verret.

La mammographie de dépistage a pour objectif de détecter un cancer du sein le plus tôt possible, pour réduire le nombre de décès, diminuer la gravité de la maladie au diagnostic et le recours à des traitements lourds.
Elle a été introduite dans un certain nombre de pays européens sur la base de huit essais randomisés. Cependant, à la lumière de ces huit études, la fourchette d’âge appropriée pour ce dépistage reste débattue. L’étude UK Age Trial est randomisée et rétrospective, rapportant ici, après un suivi de presque 23 ans de près de 161 000 patientes, une réduction significative de la mortalité par cancer du sein à 10 ans de suivi, avec 83 décès par cancer du sein dans le groupe d'intervention contre 219 dans le groupe de contrôle, [RR] 0,75 [IC 95 % : 0,58 ;0,97] ; p = 0,029), mais l’effet disparait au-delà.
Cette étude montre le bénéfice en termes de réduction de la mortalité par cancer du sein autour de l’âge de 40 ans. Cependant, les modalités de ce dépistage plus précoce ne sont pas encore précisées. L’étude MyPeBS, d’envergure internationale, menée sous la conduite de la Dr Delaloge, prévoit d’inclure 85 000 patientes de façon prospective, comparera le dépistage standard actuel à un dépistage personnalisé dont le rythme sera défini en fonction du risque de chaque patiente. Le but de cette étude est de répondre à une question simple, mais fondamentale : est-il préférable de personnaliser le type et la fréquence du dépistage du cancer du sein en fonction du risque individuel de chaque femme ?
Référence :
Duffy SW, Vulkan D, Cuckle H, et al. Effect of mammographic screening from age 40 years on breast cancer mortality (UK Age trial): final results of a randomised, controlled trial [published online ahead of print, 2020 Aug 12]. Lancet Oncol. 2020;S1470-2045(20)30398-3. doi:10.1016
Génétique
Médecine génomique de précision : une révolution en perspective dans le domaine du soin et de la prévention
Véronica Goldbarg, Olivier Caron.

Analyser l’exome de la population générale permettrait de découvrir des caractéristiques génétiques rares et des facteurs de risque de cancers non révélés par les antécédents familiaux. Deux études s’appuyant sur la vaste cohorte UK Biobank le démontrent.
L’étude anglo-saxonne UK Biobank a pour objectif de combiner des données cliniques et génétiques de plus de 500 000 individus volontaires, non sélectionnés.
Dans l’édition de Nature du 21 octobre dernier1, les investigateurs rapportent les données d’exome (Whole Exome Sequencing, WES) de 50 000 participants. Parmi les 4 millions de variants identifiés, 198 269 correspondaient à des variants « perte de fonction » (loss-of-function, LOF), presque tous avec une fréquence allélique très faible, inférieure à 1 %. La quasi-totalité des gènes étaient concernés par ces LOF. Dans la mesure où les données cliniques étaient disponibles, des associations phénotype-génotype ont pu être établies : certaines étaient connues de longue date mais de nouvelles ont aussi été caractérisées.
Surtout, près de 1 000 individus (2 %) étaient porteurs d’un variant LOF dans un des 59 gènes considérés par l’American College of Medical Genetics comme « actionnables », c’est-à-dire ayant des conséquences sur la prise en charge de la personne porteuse. Le plus souvent, il s’agissait de gènes de prédisposition au cancer (166 BRCA2, 59 BRCA1, 59 PMS2 et 52 MSH6). Cette étude précise ainsi la fréquence en population générale de ces variants LOF (0,5 % au total pour BRCA1 et BRCA2, 0,2 % pour MSH6/PMS2, impliqués dans le syndrome de Lynch). Il faut noter que seulement 40 % de ces personnes porteuses rapportaient des antécédents familiaux en lien avec la prédisposition.
L’absence de critères de sélection des personnes participantes permet par ailleurs d’évaluer la pénétrance chez les porteurs de variants pathogènes de ces gènes. Ces données sont présentées dans un article indépendant, paru dans le journal de l’American Medical Association, JAMA Netw Open2. Les risques cumulés de cancers à 75 ans sont beaucoup plus faibles que ceux décrits dans des populations sélectionnées sur l’histoire familiale (41 % pour BRCA1/BRCA2, 38 % pour le syndrome de Lynch).
Cette étude est actuellement la plus grande ressource en libre accès de données WES liées aux dossiers de santé. L’analyse WES des 450 000 participants de la UK Biobank se poursuit. Ces données clinico-biologiques issues de populations non sélectionnées seront extrêmement utiles pour affiner les recommandations de prise en charge, notamment dans la prévention des cancers.
Références :
1.Van Hout, C.V., Tachmazidou, I., Backman, J.D. et al. Exome sequencing and characterization of 49,960 individuals in the UK Biobank. Nature 586, 749–756 (2020). https://doi.org/10.1038/s41586-020-2853-0
2. Patel AP, Wang M, Fahed AC, Mason-Suares et al. Association of Rare Pathogenic DNA Variants for Familial Hypercholesterolemia, Hereditary Breast and Ovarian Cancer Syndrome, and Lynch Syndrome With Disease Risk in Adults According to Family History. JAMA Netw Open. 2020 Apr 1;3(4):e203959. doi: 10.1001/jamanetworkopen.2020.3959. PMID: 32347951.
Digestif
Un cancer du côlon pas toujours si localisé…
Léonor Benhaim.
Les cancers du côlon de stade II sont caractérisés par une absence d’extension ganglionnaire et traités par chirurgie avec un taux de guérison de 90%.
Dans certains cas le risque de récidive n’est pourtant pas négligeable. En effet un cancer du côlon de stade IIc avec atteinte locale d’un organe de voisinage va récidiver dans près de 40 % des cas. Les cancers de stade II « à haut risque » ont une définition encore controversée mais comprennent grossièrement les lésions T4, les tumeurs perforées, ou un nombre de ganglions examinés < 10. Dans ces cas particuliers, une chimiothérapie adjuvante est souvent proposée, même si son intérêt ainsi que ses modalités sont débattues dans la littérature. Lorsque l’on ajoute à cet algorithme les caractéristiques moléculaires (statut Kras, MMR, Braf, immunoscore…), les décisions de traitement peuvent devenir extrêmement complexes.
Afin de trancher cette question, un nouveau juge de paix pourrait être enfin apparu. Au-delà des considérations anatomopathologiques, la biopsie liquide pour recherche d’ADN tumoral circulant est un facteur de risque indépendant de rechute. Les travaux de recherche de la Dr Léonor Benhaim, chirurgienne robotique et colorectale à Gustave Roussy, ont permis de confirmer à partir de l’analyse de plus de 800 échantillons de plasma de patients inclus dans l’étude Algecol que la détection d’ADN tumoral circulant après chirurgie d’un cancer du côlon localisé était un indice fort de la présence d’une maladie minimale résiduelle et associé à un risque de récidive supérieur à 40 %.
Les résultats de ces travaux ont conduit à monter l’étude Circulate-II actuellement ouverte à Gustave Roussy. Dans cette étude, pour laquelle Gustave Roussy est l’un des centres investigateurs principaux, il s’agit d‘administrer une chimiothérapie uniquement pour les patients du groupe réellement à risque, c’est-à-dire chez qui l’ADN tumoral circulant est encore détectable après chirurgie. En l’absence d’ADN tumoral post-opératoire, le risque de récidive étant très faible il est proposé une simple surveillance afin d’éviter des séquelles à long terme d’une chimiothérapie inutile.
Références :
Taïeb J, Benhaim L, Laurent Puig P, Le Malicot K, Emile JF, Geillon F, Tougeron D, Manfredi S, Chauvenet M, Taly V, Lepage C, André T."Decision for adjuvant treatment in stage II colon cancer based on circulating tumor DNA: The CIRCULATE-PRODIGE 70 trial". Dig Liver Dis. 2020 Jul;52(7):730-733.
Hématologie
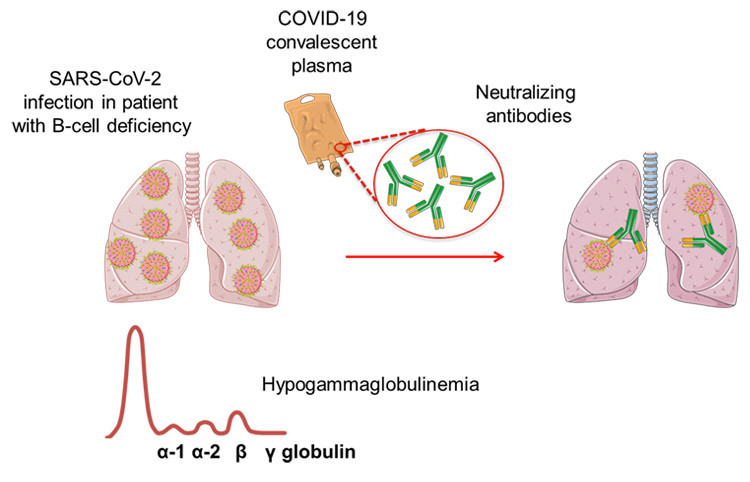
Le plasma convalescent bénéfique contre la Covid-19 chez des patients porteurs souffrant d’une hémopathie lymphoïde B.
Thomas Hueso.
Gustave Roussy, en collaboration avec Saint-Antoine, montre l’efficacité d’une transfusion de plasma convalescent pour lutter contre la Covid-19 chez des patients présentant une lymphodéplétion consécutive à une immunothérapie anti-CD20.
L’infection à SARS-CoV-2 à l’origine de la Covid-19 semble être responsable de formes plus sévères chez les patients atteints d’une hémopathie (Albiges L et al). Les patients atteints d’hémopathie lymphoïde B reçoivent dans le cadre de leurs traitements hématologiques une immunothérapie par anti-CD20 (Rituximab), molécule incontournable mais responsable d’une lymphodéplétion pouvant altérer la réponse immunitaire humorale. En effet, certains de ces patients, infectés à SARS-CoV-2, ne produisent pas suffisamment d’anticorps pour effectuer une séroconversion, même après plusieurs semaines de symptômes. En cause : l’absence de lymphocytes B circulants. Dans ce contexte, une immunité passive avec l’apport de plasma de patients convalescents comportant des anticorps neutralisants dirigés contre le SARS-CoV-2 pourrait être une approche thérapeutique utile.
En collaboration avec l’équipe d’infectiologie de l’hôpital Saint-Antoine, nous avons mené une étude rétrospective multicentrique à l’échelle nationale afin d’évaluer l’efficacité du plasma convalescent chez les patients présentant une forme chronique de la Covid-19 associée à une absence de séroconversion. Cette étude portait sur 17 malades dont 15 avaient reçu un traitement par Rituximab et 16 présentaient une alymphocytose B. Tous les patients sont devenus apyrétiques 48 heures après la perfusion de plasma et ont été sevrés de l’oxygène en moins d’une semaine. Biologiquement, cette amélioration s’accompagnait d’une rapide diminution des paramètres inflammatoires associée à une disparition de l’ARN viral dans le sang. Un des patients, présentant une Covid sévère sous ventilation mécanique, est décédé des suites d’une pneumopathie bactérienne (Hueso T et al.). Nos données suggérent que le plasma serait d’autant plus bénéfique qu’il est administré précocement dans le cadre d’une infection Covid-19.
Cette étude pilote suggère l’intérêt de la plasmathérapie chez les patients présentant un défaut de la réponse humorale dans un contexte d’infection à SARS-CoV-2. Ce travail comme preuve de concept initié à Gustave Roussy a abouti à l’ouverture de l’essai clinique Coriplasm qui est en cours au sein de l’institution.
Références :
- Albiges, L., Foulon, S., Bayle, A. et al. Determinants of the outcomes of patients with cancer infected with SARS-CoV-2: results from the Gustave Roussy cohort. Nat Cancer (2020). https://doi.org/10.1038/s43018-020-00120-5
- Convalescent plasma therapy for B-cell depleted patients with protracted COVID-19 disease. Hueso T et al. Blood. 2020 Sep 21:blood.2020008423. doi: 10.1182/blood.2020008423.PMID: 32959052
Covid-19
Covid-19 et cancer : l'expérience de Gustave Roussy
Emeline Colomba, Fanny Pommeret.
Plusieurs études ont rapporté que les patients atteints de cancer étaient plus à risque de contracter ou de développer une forme sévère de Covid-191,2. Lors de la première vague, certains facteurs associés à la gravité de la Covid-19 étaient connus3,4, mais peu de données étaient disponibles sur la spécificité des patients avec cancer. Pour aider à identifier les patients avec cancer à risque de Covid-19 sévère, et pour évaluer l'impact du virus sur la prise en charge du cancer, Gustave Roussy a mené une large étude en mars 2020.
Sur les 1 633 patients testés en interne, 196 (12 %) sont revenus positifs et 178 ont été pris en charge à Gustave Roussy. Parmi eux, 125 (70,2 %) ont été hospitalisés pour Covid-19. A cette période, aucun traitement de la Covid-19 n’avait démontré son efficacité. A Gustave Roussy, des patients ont reçu un traitement dans le cadre d’essais cliniques et d’autres hors essai. Ces derniers étaient alors traités selon un arbre décisionnel thérapeutique dynamique qui s’adaptait rapidement aux nouvelles connaissances scientifiques disponibles. Les patients ont été traités par association d'hydroxychloroquine/azithromycine (25,4 %), de lopinavir/ritonavir (2,9 %), par un immunomodulateur type Inhibiteur d'IL6 (le tocilizumab : 5,6 %) et/ou par corticothérapie (11,9 %). Parmi les 178 patients, 47 (26,4 %) se sont aggravés cliniquement et 31 sont décédés (17,4 % des patients). Toutefois, ce taux de mortalité à la Covid-19 était semblable à la mortalité des patients sans cancer admis en région parisienne. Au total le taux de mortalité sans aggravation clinique était de 73,7% (IC à 95%: 66,2; 79,9).Concernant le rôle des facteurs biologiques, la CRP, les LDH et les D-dimères étaient associés à un risque d’aggravation et/ou de décès.
Quant à l'impact du Covid-19 sur la prise en charge du cancer, on notait un retard dans la prise en charge thérapeutique de 20 jours (médiane) chez 41 % des patients, et une adaptation de la stratégie thérapeutique chez 30 % du fait d’une infection à la Covid-19.
Ces données ont mis en évidence les défis auxquels les centres de cancérologie sont confrontés et nous aide actuellement, durant cette deuxième vague, pour nous ajuster au quotidien entre la gestion des patients infectés et la nécessité d’assurer aux patients atteints de cancer l'accès aux soins essentiels.
Références :
1. Dai M, Liu D, Liu M, et al. Patients with Cancer Appear More Vulnerable to SARS-CoV-2: A Multicenter Study during the COVID-19 Outbreak. Cancer Discov. 2020;10(6):783-791. doi:10.1158/2159-8290.CD-20-0422
2. Liang W, Guan W, Chen R, et al. Cancer patients in SARS-CoV-2 infection: a nationwide analysis in China. Lancet Oncol. 2020;21(3):335-337. doi:10.1016/S1470-2045(20)30096-6
3. Guan W-J, Ni Z-Y, Hu Y, et al. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med. 2020;382(18):1708-1720. doi:10.1056/NEJMoa2002032
4. Grasselli G, Zangrillo A, Zanella A, et al. Baseline Characteristics and Outcomes of 1591 Patients Infected With SARS-CoV-2 Admitted to ICUs of the Lombardy Region, Italy. JAMA. Published online 06 2020. doi:10.1001/jama.2020.5394
Quiz
Avez-vous bien lu ce second numéro de la newsletter Good to Know ?
Abonnez-vous à la newsletter Good to Know
Ne manquez pas les prochains numéros de la newsletter Good to Know : abonnez-vous !
Crédits photos : Adobe Stock, Debiopharm, Gustave Roussy.
