
L'ACTUALITÉ EN CANCÉROLOGIE VUE PAR GUSTAVE ROUSSY
Newsletter #11 - Septembre 2021
Pédiatrie
Effet du ribociclib (inhibiteur CDK4/6) dans les cancers pédiatriques : une étude AcSé-ESMART
Birgit Geoerger

Des altérations des voies du cycle cellulaire régulées par CDK4/6 sont fréquemment retrouvées dans les cancers pédiatriques. Dans l’essai européen de médecine personnalisée AcSé-ESMART, le ribociclib, un inhibiteur de CDK4/6, a été évalué en combinaison à la chimiothérapie ou à un inhibiteur de mTOR chez des enfants et adolescents atteints de cancers avancés après analyses moléculaires.
Le ribociclib a été évalué dans cet essai de phase I/II en combinaison au topotécan et au témozolomide (bras A ; 14 patients traités) ou à un inhibiteur de mTOR, l’évérolimus (bras B ; 17 patients traités). L’inclusion dans le bras A était possible si le topotécan-témozolomide était une chimiothérapie appropriée et si les analyses moléculaires avaient identifié des altérations génétiques dans les voies du cycle cellulaire régulées par CDK4/6, tandis que l’inclusion dans le bras B était conditionnée par l’identification d’altérations génétiques dans les voies du cycle cellulaire régulées par CDK4/6 ou par la mise en évidence d’altérations affectant la voie PI3K-AKT-mTOR. Au total 80 % des patients inclus présentaient des anomalies moléculaires dans les voies d’intérêt.
Une stabilisation de la maladie fut observée chez deux des 14 patients (14 %) du bras A (un avec neuroblastome et un avec sarcome d’Ewing pendant respectivement 4 et 6 cycles) et sept des 17 patients (41 %) des patients du bras B (deux sarcomes, deux gliomes de haut grade, un médulloblastome, un neuroblastome et une leucémie aigue lymphoblastique de type T, pendant en médiane 4 cycles, soit 18 semaines sans progression). Aucune réponse objective n’a été observée.
Le profil de toxicité était comparable à celui observé chez les patients adultes lors de l’utilisation du ribociclib en combinaison, avec principalement une toxicité hématologique.
Suite à ces résultats, deux autres essais explorant le ribociclib en association au topotécan-témozolomide ou à l'évérolimus ont été initiés : le premier utilisant un schéma posologique différent et le second recrutant des patients atteints de leucémie aiguë lymphoblastique T et d'autres tumeurs malignes présentant des altérations génétiques dans les voies CDK4/6 et PI3K-AKT-mTOR.
Ce sont les premiers bras de traitement de notre étude plateforme de preuve-de concept AcSé-ESMART qui explore des médicaments ciblés chez des patients ayant des altérations dans les voies spécifiques et non-connues afin de développer des nouveaux biomarqueurs pour ces traitements.
Référence :
Bautista et al., Phase I or II Study of Ribociclib in Combination With Topotecan-Temozolomide or Everolimus in Children With Advanced Malignancies: Arms A and B of the AcSe-ESMART Trial. J Clin Oncol. 2021 Aug 4:JCO2101152. doi: 10.1200/JCO.21.01152. PMID: 34347542
Pédiatrie
Etude de phase I/II du lenvatinib associé à l’etoposide et l’ifosfamide chez les patients avec un ostéosarcome réfractaire ou en rechute (ITCC-050)
Nathalie Gaspar
Issu d’une collaboration entre Gustave Roussy, le consortium européen ITCC et le laboratoire japonais Eisai, l’essai HOPE/ITCC-050 associe pour la première fois un inhibiteur de tyrosine kinases, le lenvatinib, avec une chimiothérapie etoposide/ifosfamide. Les résultats d’efficacité semblent prometteurs et ont permis de mettre en place une seconde étude testant l’efficacité de cette combinaison de façon randomisée en première rechute d’ostéosarcome pour les enfants, adolescents et jeunes adultes, l’étude OLIE (ITCC-082), en cours actuellement.
L’ostéosarcome est la tumeur osseuse maligne primitive la plus fréquente de l’adolescent et du jeune adulte, mais reste une maladie rare (environ 150 nouveaux cas par an). Le problème principal est la survenue de rechutes notamment métastatiques qui assombrissent le pronostic. Le traitement repose sur la chimiothérapie et la chirurgie. Aucun nouveau médicament n’est utilisé en routine dans ce cancer. Récemment les médicaments inhibiteurs multi-tyrosine kinases anti-antigiogéniques administrés seuls ont démontré une efficacité dans les rechutes d’ostéosarcome.
Cette étude internationale, HOPE/ITCC-050, a été construite pour être inclusive de la population adolescente et jeune adulte, sans barrière d’âge à 18 ans, en application des principes du groupe ACCELERATE FAIR trial (Fostering Age Inclusive Research). L’étude est issue d’une collaboration entre le Dr Gaspar à Gustave Roussy, le consortium européen ITCC (Innovative Therapeutic for Child and Alodeslecent with Cancer) et le laboratoire Eisai.
L’étude HOPE/ITCC-050 testait l’association du lenvatinib avec la chimiothérapie etoposide/ifosfamide, et a démontré la faisabilité d’associer ce type de médicament agissant sur le microenvironnement de la tumeur en association avec la chimiothérapie, pour la première fois dans cette pathologie. Les résultats d’efficacité semblent aussi encourageants.
Ces résultats ont permis de mettre en place une deuxième étude internationale qui a pour objectif de tester l’étendue de l’efficacité de cette combinaison de façon randomisée, en première rechute d’ostéosarcome pour les enfants/adolescents et jeunes adultes de moins de 25 ans, l’étude OLIE.
Référence :
Gaspar N et al., Lenvatinib with etoposide plus ifosfamide in patients with refractory or relapsed osteosarcoma (ITCC-050): a multicentre, open-label, multicohort, phase 1/2 study. Lancet Oncol. 2021. Sep;22(9):1312-1321. doi: 10.1016/S1470-2045(21)00387-9.
Pédiatrie
Neuroblastome de haut risque : de guérir plus vers guérir mieux
Sandrine Haghiri, Brice Fresneau
La survie des enfants atteints de neuroblastome de haut risque a augmenté, atteignant 65 % à 3 ans, grâce à des stratégies intensives combinant chimiothérapie conventionnelle et à haute dose, chirurgie, radiothérapie et immunothérapie. Cependant, les complications tardives sont fréquentes. Petite taille, altérations de la fertilité, de l’audition et de la dentition en sont les plus fréquentes.
Entre 1980 et 2012, 439 enfants ont été traités à Gustave Roussy pour un neuroblastome de haut risque (métastatique et/ou N-MYC amplifié) par chimiothérapie à haute dose avec autogreffe de cellules souches hématopoïétiques ; parmi eux, 145 étaient vivants en rémission complète à 5 ans post-greffe et ont été inclus dans cette analyse.
L’âge médian au diagnostic était de 2,6 ans ; 96 avaient été traités avant 2000. Le suivi médian post-greffe était de 15 ans (intervalle 5-34), soit un âge médian aux dernières nouvelles de 18 ans (intervalle 7-43).
Six récidives de neuroblastome au-delà de 5 ans post-greffe, 11 seconds cancers et 9 décès ont été observés. En comparaison avec la population générale française, le risque de décès des survivants de neuroblastome de haut risque était multiplié par 19.
135 patients (93 %) souffraient d’au moins une séquelle ou complication des traitements reçus (en médiane trois/patient). L’incidence cumulée à 15 ans post-greffe des seconds cancers était de 4 % (délai médian d’apparition de 20 ans), incluant carcinomes (n=5), sarcomes (2), leucémies aiguës myéloïdes (2), mélanome (1) et gliome malin (1). Les évènements non-oncologiques observés étaient des altérations de la dentition incluant agénésies et microdonties (60 %), une perte auditive sévère (20 %), un retard de croissance (20 %), des hyperplasies nodulaires et focales hépatiques (14 %), des troubles thyroïdiens (11 %), des altérations de la fonction cardiaque (8 %) et rénale (7 %). De surcroît, 95 % des femmes souffraient d’insuffisance ovarienne prématurée après busulfan contre 33 % après une autre chimiothérapie haute dose, tandis que 96 % des hommes souffraient d’insuffisance testiculaire exocrine, quel que soit le type de chimiothérapie haute dose.
Un tel constat nous amène à proposer un suivi systématique au long cours de ces patients, y compris à l’âge adulte, dans le cadre de la consultation de suivi à long terme.
Référence :
Haghiri S, et al. Long-term follow-up of high-risk neuroblastoma survivors treated with high-dose chemotherapy and stem cell transplantation rescue. Bone Marrow Transplant 2021;56:1984–97.
Ditep
Un gel topique anti-BRAF pour traiter les rashs sous anti-EGFR
Daphné Morel, Stéphane Champiat, Loïc Verlingue

Se servir d’un anticancéreux pour soigner les effets secondaires d’un autre anticancéreux ? Une idée saugrenue et pourtant ô combien brillante, lorsque l’on se penche sur le rationnel moléculaire de cette approche « d’activation paradoxale de la voie MAPK » déclenchée par les anti-BRAF pour traiter de manière locale les rashs induits par les anti-EGFR.
Soixante-quinze à 90 % des patients traités avec des thérapies ciblées anti-EGFR développent des effets secondaires dermatologiques, principalement sous forme de rougeurs acnéiformes qui, dans certains cas, doivent amener à faire diminuer les posologies, voire à arrêter le traitement.
Du point de vue moléculaire, l’inhibition d’EGFR induit l’inhibition de phospo-ERK, ce qui réduit les capacités de régénération des keratinocytes. Il s’avère que les anti-BRAF, une autre catégorie de thérapie ciblée, interagissent avec cette même voie moléculaire, mais induisent à l’inverse l’augmentation de phosphorylation d’ERK à de faibles concentrations. Ainsi, des chercheurs ont eu l’idée de tirer parti de ce phénomène dit « d’activation paradoxale de la voie MAPK » induit par les anti-BRAF pour traiter localement les rashs induits par les anti-EGFR, grâce à un gel aqueux topique à administrer sur les lésions.
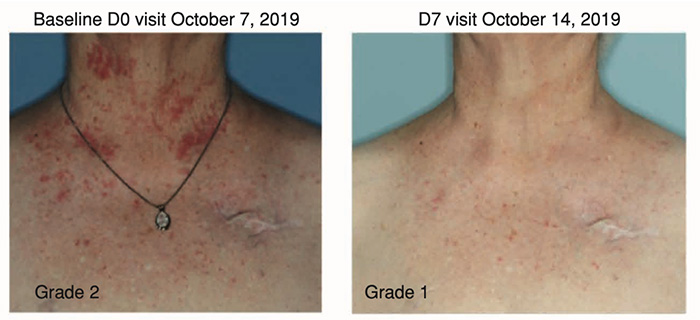
Dans cette petite cohorte de phase I, les patients atteints de rash sous anti-EGFR (cetuximab ou panitumumab ; rashs de grade 1 à 2) ont appliqué le gel contenant l’anti-BRAF (LUT014) sur leurs lésions, à des concentrations croissantes. Sept patients sur 10 (70 %) ont présenté des effets secondaires de type picotement, peau sèche et démangeaisons, de grades 1 à 2. Il n’y eu aucun effet systémique relié à l’application topique du traitement.
L’anti-BRAF topique s’est par ailleurs montré efficace aux concentrations les plus faibles (0,3 et 1 mg/g) : les patients présentant un rash de grade 2 à l’inclusion se sont tous améliorés vers un grade 1 sous quelques jours, avec des effets bénéfiques toujours observés jusqu’à 1 mois après l’arrêt de l’application. A la concentration la plus élevée (2,5 mg/g), un patient sur trois a vu ses symptômes s’empirer.
Un essai randomisé en double aveugle est en cours pour valider ces observations et prévoit d’inclure 117 patients atteints de rash de grade 2 sous anti-EGFR, traités pour cancer colorectal métastatique.
Référence :
Mario E. Lacouture et al. Reducing Skin Toxicities from EGFR Inhibitors with Topical BRAF Inhibitor Therapy. Cancer Discov 2021;11:1–10 DOI: 10.1158/2159-8290.CD-20-1847
Hématologie
Mécanismes de leucémogenèse dans le syndrome de Down
Aline Renneville, Lucie Laplane, Ileana Antony-Debré
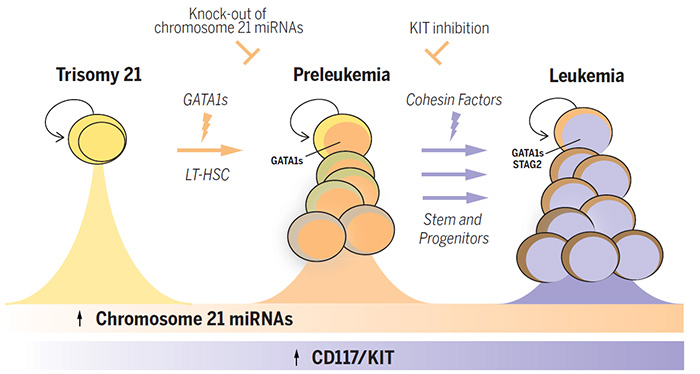
Les enfants présentant une trisomie 21 constitutionnelle (syndrome de Down) ont un risque 150 fois plus élevé de développer une leucémie. Cependant, les mécanismes par lesquels une copie supplémentaire du chromosome 21 prédispose à la leucémie restent largement méconnus. Dans cette étude, Wagenblast et al. ont identifié les mécanismes responsables d’une pré-leucémie et ceux qui déterminent la progression en véritable leucémie.
Les leucémies sont les cancers les plus fréquents chez les enfants, les premières altérations génétiques se produisant souvent in utero. Ces événements initiateurs génèrent des cellules pré-leucémiques, qui sont les précurseurs de la leucémie qui survient après la naissance.
Les enfants atteints de syndrome de Down ont globalement un risque 150 fois plus élevé de développer une leucémie aiguë myéloïde (LAM) au cours des 5 premières années de la vie. La leucémogenèse dans le contexte du syndrome de Down représente donc un modèle pour étudier les différentes phases du développement de la leucémie chez l’homme. A l’aide de modifications génétiques introduites par le système CRISPR/Cas9 dans les cellules souches et progénitrices hématopoïétiques dérivées du foie fœtal humain et d’expériences de transplantation dans des souris receveuses, Wagenblast et al. ont développé un modèle permettant de caractériser les événements moléculaires et les types cellulaires à l’origine du développement de la leucémie dans un contexte de trisomie 21.
Leurs résultats montrent que les mutations du gène GATA1 provoquent un état pré-leucémique transitoire lorsqu'elles ont été introduites dans des cellules trisomiques souches hématopoïétiques. De plus, dans ces cellules, 3 microARN (miR) localisés sur le chromosome 21, miR-99a, miR-125b-2, et miR-155, contribuent à l’initiation de la pré-leucémie.
En revanche, la phase de progression en véritable LAM est indépendante de la trisomie 21 et provient de divers types de cellules souches et progénitrices qui ont acquis des mutations additionnelles, en particulier des mutations inactivatrices des gènes du complexe cohésine comme le gène STAG2.
Enfin, cette étude suggère, sur la base de résultats prometteurs obtenus sur des modèles de souris, que l’utilisation d’inhibiteurs de KIT tels que le dasatinib ou le ripretinib pourrait permettre de cibler les cellules souches pré-leucémiques et ainsi représenter une stratégie de prévention précoce pour freiner la progression en véritable leucémie.
Référence :
Wagenblast E et al. Mapping the cellular origin and early evolution of leukemia in Down syndrome. Science. 2021 Jul 9;373(6551):eabf6202. doi: 10.1126/science.abf6202.
Abonnez-vous à la newsletter Good to Know
Ne manquez pas les prochains numéros de la newsletter Good to Know : abonnez-vous !
Crédits photos : Adobe Stock, Gustave Roussy.
