Remodelage de la chromatine, réparation de l’ADN et épigénétique
Cette équipe est rattachée à l'UMR 981 - Prédicteurs moléculaires et nouvelles cibles en oncologie
L’ADN, code génétique qui programme la cellule, est similaire aux lettres des mots d’un livre. Pour qu’une histoire soit compréhensible, il faut que les mots soient correctement orthographiés et espacés, et que le texte soit pourvu d’une ponctuation correcte. Dans la cellule cancéreuse, l’ADN accumule les fautes d’orthographe et la ponctuation est altérée. Ces phénomènes résultent respectivement de défauts de réparation de l’ADN et d’une dérégulation de l’épigénétique. Ils aboutissent au cancer car faussent le programme de la cellule.
Les objectifs de notre équipe sont de :
- comprendre les défauts de réparation de l’ADN et la dérégulation épigénétique ;
- identifier de nouveaux traitements pour spécifiquement cibler ces anomalies dans la cellule cancéreuse ;
- évaluer, au travers de protocoles cliniques, les traitements les plus prometteurs chez les patients grâce à la collaboration avec l’Hôpital Gustave Roussy.
Nous nous intéressons particulièrement au cancer du poumon et aux sarcomes, mais étudions aussi d’autres types tumoraux.
Thèmes de recherche de l’équipe
Le remodelage de la chromatine est un processus qui permet à la cellule de moduler l’expression de ses gènes sans modifier son code génétique. Il joue un rôle essentiel dans la survenue du cancer, la progression tumorale et la résistance aux traitements. Le complexe SWI/SNF (Switch / Sucrose Non-Fermentable) est un acteur majeur de ce remodelage.
Il n’existe actuellement aucun traitement enregistré ciblant les tumeurs présentant un défaut de SWI/SNF, qui représentent plus de 20% des cancers. Notre équipe cherche donc à identifier de nouveaux traitements pour cibler spécifiquement ces tumeurs et proposer de nouvelles approches thérapeutiques aux patients.
Plus spécifiquement, nos projets visent à :
- Rechercher de façon systématique de nouveaux traitements potentiels à travers la réalisation de criblages à haut débit sur des modèles cellulaires
- Comprendre le mécanisme d’action des molécules candidates et explorer les mécanismes de résistance associés
- Évaluer l’effet chez l’animal des molécules candidates
- Développer le protocole clinique correspondant en liaison avec Gustave Roussy hôpital, grâce au double rôle de médecin et chercheur de la responsable d’équipe
- Développer les biomarqueurs nécessaires à l’identification des patients pouvant bénéficier des approches identifiées au laboratoire
Nous nous concentrons en priorité sur le rôle de SWI/SNF dans la réparation de l’ADN et l’immunité antitumorale, en particulier dans le cancer du poumon, le cancer du rein et les sarcomes. Nous étudions également comment les défauts de réparation de l’ADN et la dérégulation épigénétique influencent l’immunité antitumorale, en utilisant des modèles précliniques cellulaires ou animaux et des échantillons de tumeurs de patients. Notre approche est multidisciplinaire et allie des techniques de biologie moléculaire, biologie cellulaire, imagerie, bioinformatique et caractérisation moléculaire multi-omics à haut débit.
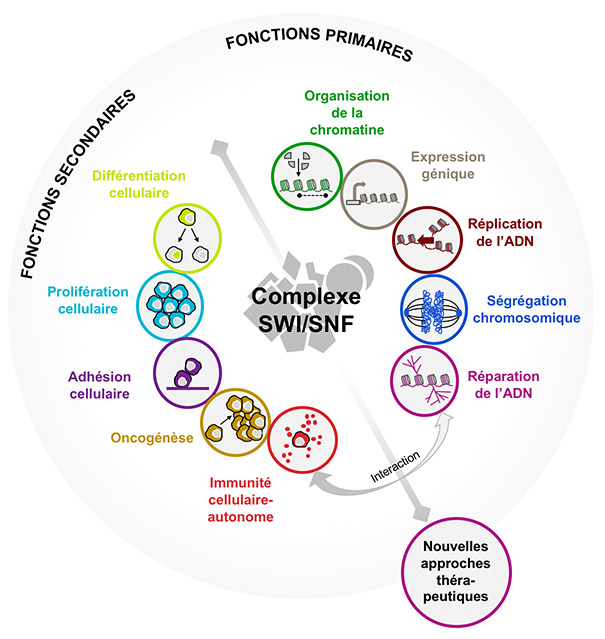
Figure récapitulative : Résumé des multiples fonctions dans lesquelles SWI/SNF est impliqué, pouvant faire l’objet de nouvelles approches thérapeutiques dans le traitement du cancer. Notre équipe se focalise en particulier sur la réparation de l’ADN et l’immunité antitumorale. D’après Chabanon et al, Semin in Cancer Biology 2019.
