
Janvier
Ouverture de la station Villejuif-Gustave Roussy

Samedi 18 janvier, la station de métro Villejuif–Gustave Roussy, située au pied de l’Institut, a été inaugurée. Desservie par la ligne 14, elle place désormais Gustave Roussy à 10 minutes de l’aéroport d’Orly et à 15 minutes du centre de Paris. Une avancée majeure en matière d’accessibilité, qui s’inscrit dans le développement du Campus Grand Parc autour de l’Institut.
► En savoir plusOASIS : un programme européen pour optimiser les anticorps conjugués

Lancé en janvier 2025, OASIS est un programme international de recherche biomédicale coordonné par Gustave Roussy. Il réunit un consortium de 12 partenaires à travers l’Europe, unis par un objectif commun : améliorer le traitement du cancer. OASIS est un programme centré sur l’optimisation des anticorps conjugués (ADCs), une nouvelle classe de thérapies contre le cancer. Ces traitements innovants ciblent les cellules cancéreuses avec précision, réduisant ainsi les dommages aux tissus sains. Coordonné par Gustave Roussy et dirigé par la Dr Barbara Pistilli, le projet vise à développer des outils permettant aux cliniciens de choisir l'ADC le plus adapté à chaque patient, en tenant compte de ses caractéristiques cliniques et de la biologie de sa tumeur.
► En savoir plusFévrier
Le Président de la République Emmanuel Macron pose la première pierre du futur bâtiment de recherche

Le 4 février, journée mondiale de lutte contre le cancer, a été marqué par la visite à Gustave Roussy du président de la République Emmanuel Macron et de la Première dame Brigitte Macron, accompagnés d’Élisabeth Borne, ministre d’État, ministre de l’Éducation nationale, de l’Enseignement supérieur et de la Recherche, de Catherine Vautrin, ministre du Travail, de la Santé, des Solidarités et des Familles, de Philippe Baptiste, ministre délégué à l’Enseignement supérieur et à la Recherche, de Yannick Neuder, ministre chargé de la santé et de l’accès aux soins, de Clara Chappaz, ministre déléguée chargée de l’Intelligence artificielle, en présence d’Etienne Stoskopf, préfet du Val-de-Marne, de Marc Guillaume, préfet d’Île-de-France, de Valérie Pécresse, présidente du Conseil régional d’Île-de-France, d’Olivier Capitanio, président du Conseil départemental du Val-de-Marne, de Pierre Garzon, maire de Villejuif, de Michel Leprêtre, président de l’Établissement public territorial Grand Orly Seine, de Denis Robin, Directeur Général de l’ARS Île-de-France, du Pr Fabrice Barlesi, directeur général de Gustave Roussy et du Pr Éric Vivier, président du Paris-Saclay Cancer Cluster. Lors de cette visite officielle, le président de la République Emmanuel Macron et le Pr Fabrice Barlesi ont posé la première pierre du nouveau bâtiment de recherche de l’Institut, dont la livraison est prévue pour fin 2028.
► En savoir plusL’édition inaugurale du Prix Gustave Roussy remis au Pr Charles Swanton

Pour sa première édition, le Prix Gustave Roussy, créé par la Fondation Gustave Roussy avec le soutien des Laboratoires Pierre Fabre en tant que mécène fondateur, a été remis au Pr Charles Swanton. Figure mondiale de la biologie évolutive du cancer, le Pr Swanton est reconnu pour ses travaux pionniers sur la dynamique des tumeurs et l’hétérogénéité tumorale, qui ouvrent de nouvelles perspectives pour des traitements plus personnalisés.
► En savoir plusMars
Transatlantic Exchanges : renforcer les ponts scientifiques avec le Dana-Farber

Le 19 mars, Gustave Roussy a co-organisé à Paris la 4e édition des Transatlantic Exchanges avec le Dana-Farber Cancer Institute. Coprésidée par le Pr Karim Fizazi et le Dr Toni Choueiri, cette journée scientifique était consacrée aux thérapies par radiopharmaceutiques, un champ en plein essor. L’événement illustre la vitalité des collaborations internationales de Gustave Roussy au service de l’innovation et des patients.
► En savoir plusLancement des premiers essais cliniques de phase I en médecine nucléaire

L’Autorité de Sûreté Nucléaire et Radioprotection (ASNR) et l’Agence Régionale de Santé (ARS) Île-de-France ont autorisé Gustave Roussy à mener des essais cliniques de phase I en médecine nucléaire, soit la première étape du parcours de validation d’un nouveau traitement. L’Institut est donc désormais en capacité d’évaluer des radioligands innovants qui sont administrés pour la première fois ou en phase très précoce chez l’humain.
► En savoir plusChirurgie robotique : une première française avec le robot da Vinci Single Port
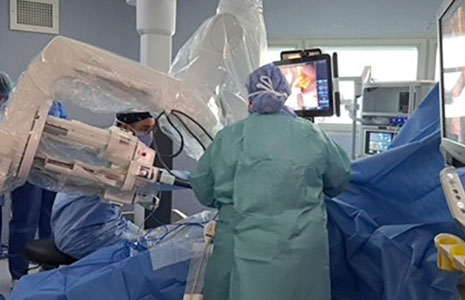
L’équipe de chirurgie viscérale de Gustave Roussy a réalisé une colectomie droite et une hépatectomie épaulée par l’appareil de chirurgie robot-assistée da Vinci Single Port. Il s’agit d’une première en France. La colectomie est une intervention chirurgicale visant à retirer une partie ou la totalité du côlon. Une hépatectomie consiste à retirer une partie du foie des patients.
► En savoir plusGustave Roussy partenaire du Printemps des Poètes

À l’occasion du Printemps des Poètes, événement culturel majeur soutenu par le Ministère de la Culture et le Centre national du livre Gustave Roussy, en tant que partenaire officiel, a lancé son premier concours de poésie intitulé Faites fleurir vos plumes. Dans ce cadre, l’Institut a accueilli la Ministre de la Culture Madame Rachida Dati, qui a récompensé les sept lauréats. Ouvert à tous, patients, aidants et proches, soignants, personnels, ce concours avait pour objectif de stimuler l’expression artistique et de permettre à chacun de partager sa créativité, tout en célébrant la poésie sous toutes ses formes.
► En savoir plusCancers ORL : Gustave Roussy mobilisé pour la campagne Rouge-Gorge

Du 31 mars au 4 avril, Gustave Roussy a participé à la campagne nationale Rouge-Gorge, dédiée à la sensibilisation aux cancers de la gorge. À cette occasion, le comité ORL / Tête et cou de l’Institut a mené plusieurs actions de prévention, dont un stand d’information à La Défense le 6 mai.
► En savoir plusAvril
Lancement du programme européen DOSELIA : l’intelligence artificielle au service de la radiothérapie pédiatrique

DOSELIA, projet de recherche européen collaboratif incluant des institutions de premier plan et coordonné par Gustave Roussy, vise à améliorer la radiothérapie pédiatrique en réduisant les effets secondaires des traitements jusqu’à l’âge adulte. Cette initiative entend optimiser la prise en charge des jeunes patients atteints de cancer, en intégrant des technologies de pointe pour mieux évaluer et limiter l’exposition des tissus sains aux rayonnements.
► En savoir plusOuverture d’un premier établissement sous licence de marque Gustave Roussy en Égypte

Gustave Roussy a inauguré au Caire son premier établissement sous licence de marque, un centre de 300 lits dédié aux cancers de l’adulte, franchissant ainsi une étape majeure dans le rayonnement international de l’Institut. Une première licence de marque qui devrait être suivie d’autres prochainement.
► En savoir plusTrois premières chaires d’excellence pour accélérer la recherche en oncologie

La Fondation Gustave Roussy a lancé un ambitieux programme de chaires d’excellence destiné à attirer et fidéliser des chercheurs de tout premier plan en oncologie. Trois premières chaires, déjà opérationnelles, sont portées par des scientifiques de renommée internationale : Éric Vivier (cellules NK), Florent Ginhoux (cellules myéloïdes et cancers pédiatriques) et Alexandre Detappe (nanothérapies). En offrant un environnement de recherche d’excellence au cœur du Paris-Saclay Cancer Cluster, ce programme vise à accélérer les découvertes majeures et leur traduction en nouvelles options thérapeutiques pour les patients.
► En savoir plusGustave Roussy au congrès de l’AACR 2025

Du 25 au 30 avril à Chicago, Gustave Roussy a participé au congrès de l’American Association for Cancer Research (AACR), rendez-vous international majeur de la recherche scientifique et translationnelle en cancérologie. Aux côtés de l’ASCO et de l’ESMO, l’AACR figure parmi les temps forts mondiaux de l’oncologie, mettant en lumière les avancées qui transforment la recherche en applications cliniques au bénéfice des patients.
► En savoir plusMai
Semaine de la Recherche Clinique : focus sur la radiologie interventionnelle

Du 19 au 25 mai, Gustave Roussy a organisé la 5e édition de sa Semaine de la Recherche Clinique. Cette édition mettait à l’honneur la radiologie interventionnelle, une spécialité mini-invasive permettant notamment de traiter des tumeurs ou des métastases et de réaliser des biopsies, au cœur des avancées en oncologie.
► En savoir plusGustave Roussy au congrès de l’ASCO 2025

À l’occasion du Congrès de l’ASCO, qui s’est tenu du 30 mai au 4 juin 2025, Gustave Roussy a vu plus d’une centaine d’études menées ou co-menées par ses médecins-chercheurs sélectionnées et présentées, témoignant de son rôle majeur dans l’innovation thérapeutique en oncologie.
► En savoir plusUne campagne de recrutement inédite dans le métro parisien

À l’occasion de l’ouverture de la station « Villejuif – Gustave Roussy » sur la ligne 14, l’Institut a déployé pour la première fois une campagne d’affichage dans le métro pour attirer des talents dans plus de 250 métiers et renforcer ainsi ses équipes.
► En savoir plusJuin
Un an du lancement du programme FRESH : plus de 5 000 patients bénéficiaires

Un an après son lancement, le parcours FRESH a permis à plus de 5 000 patients d’accéder au profilage génomique de leur tumeur par simple prise de sang, réduisant ainsi les inégalités territoriales et facilitant l’accès à des traitements innovants et personnalisés.
► En savoir plusJuillet
TALAPRO-2 : une avancée clé dans les cancers de la prostate

L’essai TALAPRO-2, coordonné par Gustave Roussy, a montré que l’association d’un nouveau médicament ciblé et d’un traitement hormonal améliore significativement les résultats chez certains patients atteints de cancer de la prostate, notamment ceux porteurs d’une mutation génétique spécifique (BRCA2).
► En savoir plusAoût
La chercheuse Sophie de Carné nommée Young Leader franco-britannique

Sophie de Carné, chercheuse à Gustave Roussy, a été sélectionnée par le conseil franco-britannique parmi les Young Leaders, une promotion annuelle prestigieuse qui rassemble une nouvelle génération de talents prometteurs issus de secteurs variés tels que la recherche, l’innovation, la culture et l’économie. Cette reconnaissance souligne son engagement et son potentiel à renforcer la coopération scientifique entre la France et le Royaume-Uni, tout en mettant en lumière ses travaux de pointe en oncologie.
► En savoir plusLauréats INSERM : Gustave Roussy à l’honneur avec deux chercheurs distingués

Chaque année, les principaux organismes de recherche publique français recrutent leurs nouveaux chargés de recherche titulaires via un système de concours très sélectif. Cette année, deux chercheurs de Gustave Roussy figurent parmi les lauréats du concours de l'Institut national de la santé et de la recherche médicale (Inserm) : Stéphanie Corgnac et Inigo Landa.
► En savoir plusSeptembre
De nouveaux laboratoires pour les équipes de recherche de Gustave Roussy

Sept équipes de chercheurs ont emménagé dans de nouveaux locaux au sein du bâtiment Lab116 Perelis, situé juste à côté de Gustave Roussy, sur le Campus Grand Parc.
► En savoir plusGustave Roussy, toujours premier centre français et européen de lutte contre le cancer

Le magazine américain Newsweek a confirmé la place de Gustave Roussy comme premier centre français et européen en oncologie, et parmi les meilleurs mondiaux.
► En savoir plusUne recherche ambitieuse sur les cancers pédiatriques incurables

Gustave Roussy, engagé depuis toujours contre les cancers de l’enfant, poursuit ses efforts pour améliorer le pronostic des tumeurs pédiatriques incurables. En 2025, l’Institut met à l’honneur deux programmes majeurs : le suivi des gliomes cérébraux agressifs avec le programme BIOMEDE, et une thérapie cellulaire innovante contre le neuroblastome, combinant cellules CAR-T et macrophages modifiés. Soutenue par la Fondation Gustave Roussy et la générosité du public, cette mobilisation vise à offrir de nouvelles chances de guérison aux jeunes patients.
Octobre
Octobre Rose : agir ensemble contre le cancer du sein

À l’occasion d’Octobre Rose, Gustave Roussy a mis en avant la reconstruction mammaire immédiate dans une nouvelle opération de communication. Grâce à la campagne philanthropique 50 nuances de rose, un programme d’intelligence artificielle dédié au cancer du sein a été financé. Par ailleurs, la course solidaire Odysséa a battu un record en collectant plus d’un million d’euros au profit de la recherche menée à Gustave Roussy.
► En savoir plusGustave Roussy au congrès ESMO 2025

Organisé à Berlin du 17 au 21 octobre 2025, le congrès de la Société Européenne d’Oncologie Médicale (ESMO) a une nouvelle fois constitué un temps fort de la recherche mondiale en oncologie, en rassemblant plus de 31 000 experts internationaux. Pendant cinq jours, les dernières avancées thérapeutiques et les résultats d’essais cliniques majeurs, susceptibles de faire évoluer la prise en charge de nombreux patients, y ont été présentés.
L’expertise des médecins-chercheurs de Gustave Roussy y a été largement reconnue, avec la présentation de 60 études scientifiques couvrant un large spectre de thématiques, des mécanismes de résistance aux thérapies innovantes aux enjeux d’égalité en oncologie.
► En savoir plusNovembre
Novembre masculin : un mois dédié à la santé des hommes et au dépistage des cancers

Gustave Roussy a lancé sa campagne « Prends soin de tes bijoux » pour sensibiliser le grand public aux cancers masculins, qui représentent chaque année près de 30 000 nouveaux cas en France, dont une large majorité concerne le cancer de la prostate.
► En savoir plusRadio Classique décerne le Prix de l’Innovation à Gustave Roussy

Gustave Roussy a été honoré du Prix de l’Innovation lors des Trophées de l’Entreprise organisés par Radio Classique. Cette distinction récompense l’excellence et la capacité de l’Institut à repousser les frontières de la recherche et des soins contre le cancer.
► En savoir plusNovembre thoracique : des avancées dans le cancer du poumon

Pour la première fois en 50 ans, une étude dirigée par la Dr Patricia Pautier et publiée dans The New England Journal of Medicine, a mis en évidence une nouvelle thérapie qui améliore la survie des patients atteints de léiomyosarcome avancé. Cette avancée significative ouvre de nouvelles perspectives pour le traitement des sarcomes des tissus mous.
► En savoir plusDécembre
Gustave Roussy progresse dans le classement du magazine Le Point

Gustave Roussy progresse dans le classement des meilleurs hôpitaux français publié par le magazine Le Point. L’Institut figure 11 fois dans le top 10 pour plusieurs spécialités en cancérologie, dont 8 fois dans le top 5. À noter : Gustave Roussy est premier pour la prise en charge des cancers ORL depuis plus d’une décennie et se classe notamment en 2nde position dans la chirurgie des cancers du sein. Une performance qui reflète l’engagement quotidien de l’ensemble des équipes de Gustave Roussy.
► En savoir plus